醫生正在利用深度學習算法幫助患者治療癌癥
▲ 液體活檢具有顯著的成本效益,能夠極大簡化活組織檢查的整體流程
根據維基百科的描述,最早的活檢診斷源自十一世紀的一位阿拉伯醫生之手。“活組織檢查”biopsy這一術語中的bios意為生命,源自希臘語中的opsis,意為視覺。這種方法最初于十九世紀引入,從那時起,醫學研究人員與從業者們先后開發出多種技術,從而對活體器官或組織進行檢查,并通過進一步觀察判斷患者體征。以腸活檢管為代表的各類現代器械,如今已經能夠從難以接近甚至危險性極高的身體部位處提取樣本。
在以上案例當中,這種組織取樣過程具有侵入性且執行方法相當復雜,不僅會給患者造成經濟負擔,同時也會在精神層面帶來額外的壓力。而液體活檢則是一種新興且前景相當光明的活檢技術,能夠檢測并分離循環腫瘤DNA與外泌體,并將其作為癌癥患者基因組與蛋白質組學信息的來源。
可以看到,每一種新興技術都在有效性與準確性等領域面臨著多種技術障礙,但新技術的開發與新一代測序分析的出現已經允許我們在各類環境當中廣泛應用液體活檢方法。液體活檢最初僅被用于診斷后跟蹤,但如今相關數據已經被應用于癌癥診斷,包括篩查,更重要的是其可用于預測患者對于特定治療方法的反應或抗性。具體來講,憑借更簡單易行的液體活檢機制,醫師可以通過這種方法更輕松地檢測標靶基因中的特定突變。如此一來,醫生將能夠利用更多數據對特定療法進行實時分析,并據此判斷療法的適當性或者確定繼發性耐藥狀況,從而盡早診斷疾病的進展情況。
自從1869年人們首次從血液循環當中發現腫瘤細胞以來,應用生物技術從異質血液成分當中分離出CTC已經取得了實質性進展。然而,液體活檢在實際操作層面仍然面臨一系列阻礙,例如其特異性與敏感性無法令人滿意、缺乏標準化、以及過高的經濟與人力資源成本等等。事實上,由于目前能夠從患者體內收集到的CTC、ctDNA以及EXO濃度較低,因此分析結果的特異性以及敏感性有時并不能滿足準確診斷的要求。
>>> 我們已經處于液體活檢方法的第二階段
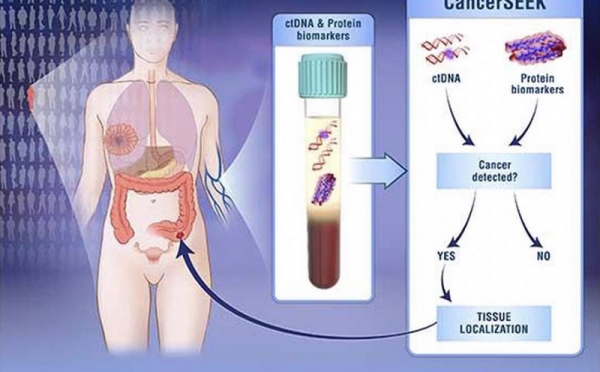
液體活檢的最初實現方法集中在ctDNA或者蛋白質層面。但正如約翰霍普金斯大學Kimmel癌癥中心腫瘤學教授Nickolas Papadopoulos博士在一篇論文當中所解釋的那樣:“早期癌癥患者血液當中的ctDNA含量非常低,只在所有無細胞DNA總量當中占比0.01%。”因此如果利用患者的血液進行硬性測試,那么結果當中可能包含大量隨機結論。此外,也有不少癌癥并不會將腫瘤DNA“脫落”至血液循環當中;因此如果單純測定ctDNA因子,那么醫療人員將無法檢測到某些癌癥;對于另一些癌癥,雖然能夠測試到,但敏感性仍然無法令人滿意。
雙ctDNA與蛋白質液體活檢研究的第一份報告,將存在KRAS基因突變的血液檢測與蛋白質生物標志物加以結合,用以確定這些標志物的組合是否確實優于任何單一標志物。報告的胰腺導管腺癌患者(PDAC)與醫療人群之間的敏感性比例為64%,特異性為99.5%。可以看到,這種兩相對照的判斷方式要遠優于任何單一因素判斷方法。
▲ CancerSEEK給出的報價低于500美元,這種雙因素液體活檢有望成為液體活檢市場上的理想解決方案
第二份報告則重點關注其它早期癌癥,包括卵巢癌、肝癌、胃癌、胰腺癌、食道癌、結腸直腸癌、肺癌與乳腺癌等。此項測試名為CancerSEK,中位敏感度為70%(乳腺癌最低,為33%;卵巢癌最高,為98%),所有受試癌癥的特異性均高于99%。
利用機器學習算法,診療人員甚至能夠借此定位腫瘤,且相關結論通過常規測試(例如乳房X射線照片或結腸鏡檢查)得到了證實。Papadopoulos博士表示,“這項檢測實際上具有泛癌癥診斷能力,我們將繼續推動更進一步的探索。”研究人員們認為,CancerSEEK的最終成本可能會低于500美元,與目前的篩查癌癥測試類似,并可通過與其它腫瘤生物標志相結合以進一步提高其特異性與敏感性。Papadopoulos博士在討論這種測試的未來前景時總結稱,“我們正在開展前瞻性研究以測試CancerSEEK的實際效果。這是一種真正值得評估且具有臨床適用性的測試方法。”
2016年,全球液體活檢市場的總規模約為2349萬美元,但隨著資金不斷注入這一領域,預計其總規模將在2023年超過12億美元。
▲ 機器學習將成為下一代測序方法中的指數因子
>>> 下一代測序將利用機器學習作為指數因子
與針對單一遺傳改變特征的檢測相反,NGS旨在記錄多種癌癥亞型當中存在的遺傳改變跡象。此外,NGS還能夠檢測出多種可能引發腫瘤的突變,并鑒定可能在治療之后從已存在的克隆特征進化而來的抗性機制。正如意大利那不勒斯Istituto Nazionale Tumori轉化研究部主任Nicola Normanno教授所言,“通過液體活檢檢測ctDNA確實具有很好的效果。通過NGS平臺,我們將能夠提取出更為深入的分子級表征。”但在一項關于NGS液體活檢的研究當中,他和他團隊強調稱他們還需要解決一系列具體挑戰。“我們目前研究的中心點在于,我們需要更多研究特異性與敏感性,以便將NGS液體活檢方法引入診所。之所以關注這方面問題,是因為血液樣本當中的ctDNA水平一般較低,此外NGS檢測到的潛在癌變也有可能來自克隆性造血——而非與腫瘤相關的DNA。因此,我們需要更深入地了解ctDNA的生物學特征,從而改進這項技術。”
在另一方面,NGS液體活檢的關鍵優勢,在于能夠檢測由整體腫瘤引起的血液突變,從而克服腫瘤異質性的問題。這種方法還可用于監測治療反應與耐藥性的變化情況。在被問及NGS液體活檢的其它潛在用途時,Normanno教授談到了借此評估腫瘤突變負荷(TMB)的可能性——TMB目前被廣泛視為應對免疫治療的潛在生物標志。
>>> 我們是否即將迎來轉折點?
液體活檢市場的規模證明,我們目前尚處于該項技術的早期發展階段。首批商業化測試必須能夠證明自身的有效性,同時說服醫生、臨床中心以及各國際組織對具體流程進行標準化,從而將信號與噪聲隔離開來,最終為整個醫療保健行業創造真正的價值。
機器學習算法的大量應用,為我們帶來了提高測試結果準確性的可能,也能夠將特定癌癥類型與患者獨特的基因身份聯系起來,繼而提供為其量身定制的治療選擇。此外,這種微創性質的檢測方法也能夠顯著降低重復測試所帶來的心理負擔,幫助本就壓力巨大的患者以更積極的心態面對漫長的診斷與治療過程。